Descubren el 'punto débil' del patógeno multirresistente conocido como MRSA
- El estafilococo dorado resiste a todos los antibióticos
- Los científicos han descubierto el mecanismo por el que es mutirrestente
- El hallazgo puede permitir el desarrollo de un antibiótico que sea efectivo
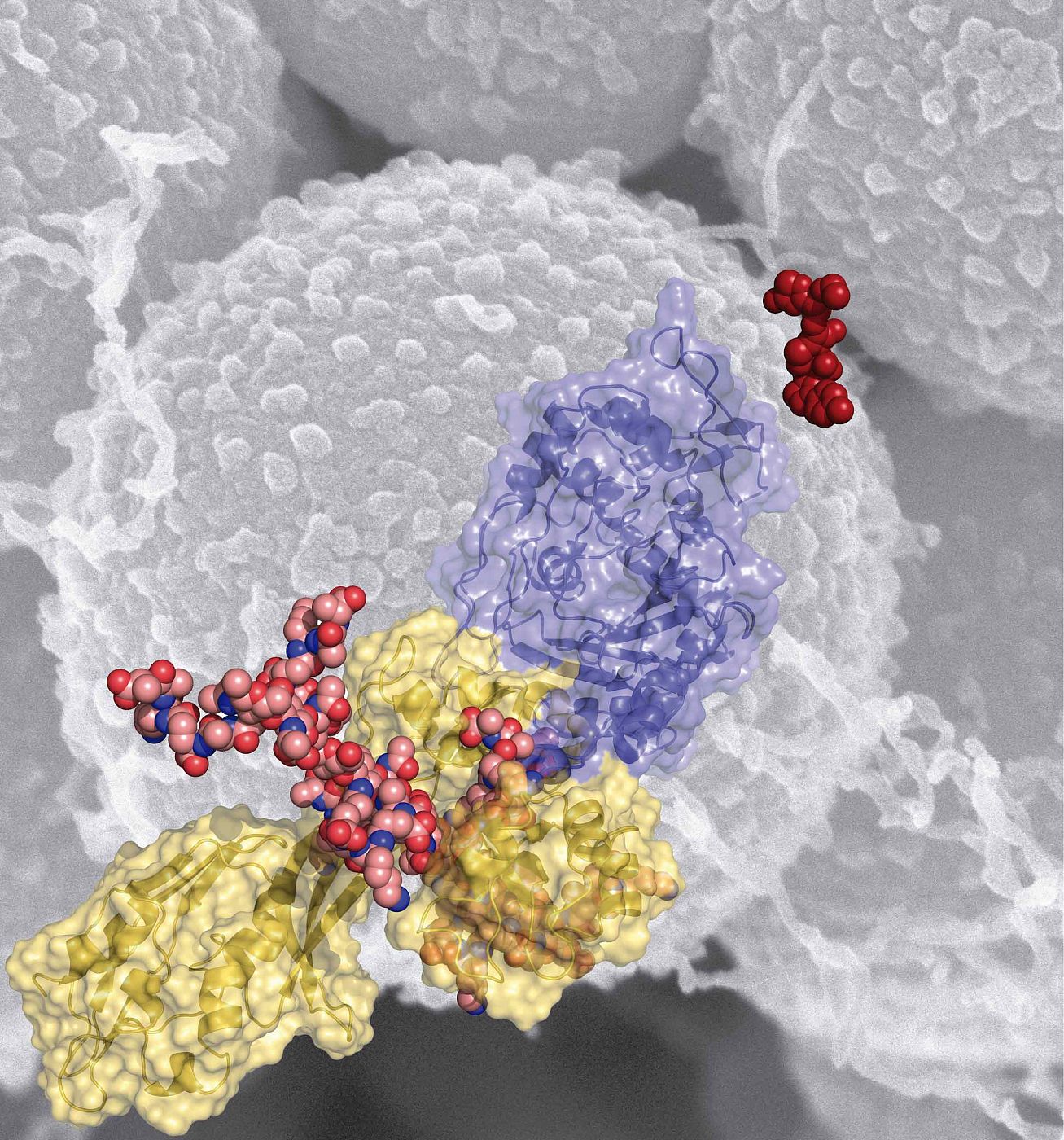

El estafilococo dorado, también conocido por MRSA en sus siglas en inglés, es un patógeno multirresistente que desarrolla resistencia a la mayor parte de los antibióticos convencionales. Una investigación, realizada por el Consejo Superior de Investigaciones Científicas (CSIC) y la Universidad de Notre Dame, en Indiana (EE. UU.), ha caracterizado el mecanismo por el que ocurre ese fenómeno.
“Este patógeno es el responsable de un gran número de enfermedades que van desde afecciones en la piel e infecciones en heridas, hasta neumonías y septicemias que pueden provocar la muerte", ha explicado el investigador del CSIC del Instituto de Química-Física Rocasolano, Juan Hermoso al CSIC.
Hermoso ha indicado que las infecciones relacionadas con MRSA son de las más importantes entre los patógenos multirresistentes debido a la alta mortalidad que causa anualmente.
Según datos explicados por Hermoso y recogidos en Estados Unidos, el estafilococo dorado causa más de de 80.000 infecciones cada año, de las cuales más de 11.000 acaban con el fallecimiento del paciente.
La resistencia del estafilococo dorado
Según este estudio, la clave de la resistencia de MRSA a los antibióticos beta-lactámicos (como los derivados de la penicilina) es la proteína PBP2a, que está implicada en la biosíntesis de la pared bacteriana del patógeno.
En bacterias susceptibles a estos antibióticos las proteínas encargadas de la construcción de dicha pared se ven bloqueadas por los agentes y dejan de reproducirse. Sin embargo, en el caso del estafilococo dorado, PBP2a es insensible a ese bloqueo y permite al patógeno continuar con su ciclo celular aún en presencia de antibióticos.
El mecanismo que permite a PBP2a resistir a la mayoría de los antibióticos está relacionado con un sitio alósterico, es decir, un sitio muy lejano al sitio activo de la enzima pero capaz de controlar su activación.
Mediante cristalografía de rayos X los investigadores han determinado la estructura tridimensional de PBP2a en complejo con ceftarolina, uno de los pocos antibióticos que son hoy efectivos frente al MRSA.
“Esta estructura ha revelado que la unión de la ceftarolina con el sitio alostérico produce toda una serie de cambios en la proteína que la activan y la dejan sensible a la inactivación por parte del antibiótico. Es como un interruptor que activa la enzima: los antibióticos convencionales no pueden encender ese interruptor, por lo que son inocuos para el patógeno. Este estudio describe cómo se produce este encendido y abre una nueva vía para el desarrollo de nuevos antibióticos”, añade Hermoso.
Un problema de salud mundial
La resistencia antimicrobiana supone uno de los problemas más serios para la salud a nivel mundial en la actualidad. “La falta de eficacia de los antibióticos incapacita nuestra manera de luchar contra las enfermedades infecciosas y de hacer frente a las complicaciones comunes en pacientes sometidos a quimioterapia en tratamientos de cáncer, en diálisis y en operaciones quirúrgicas, especialmente en aquellas de trasplante de órganos para las cuales la capacidad de tratar estas infecciones secundarias es vital”, resalta el investigador del CSIC.



