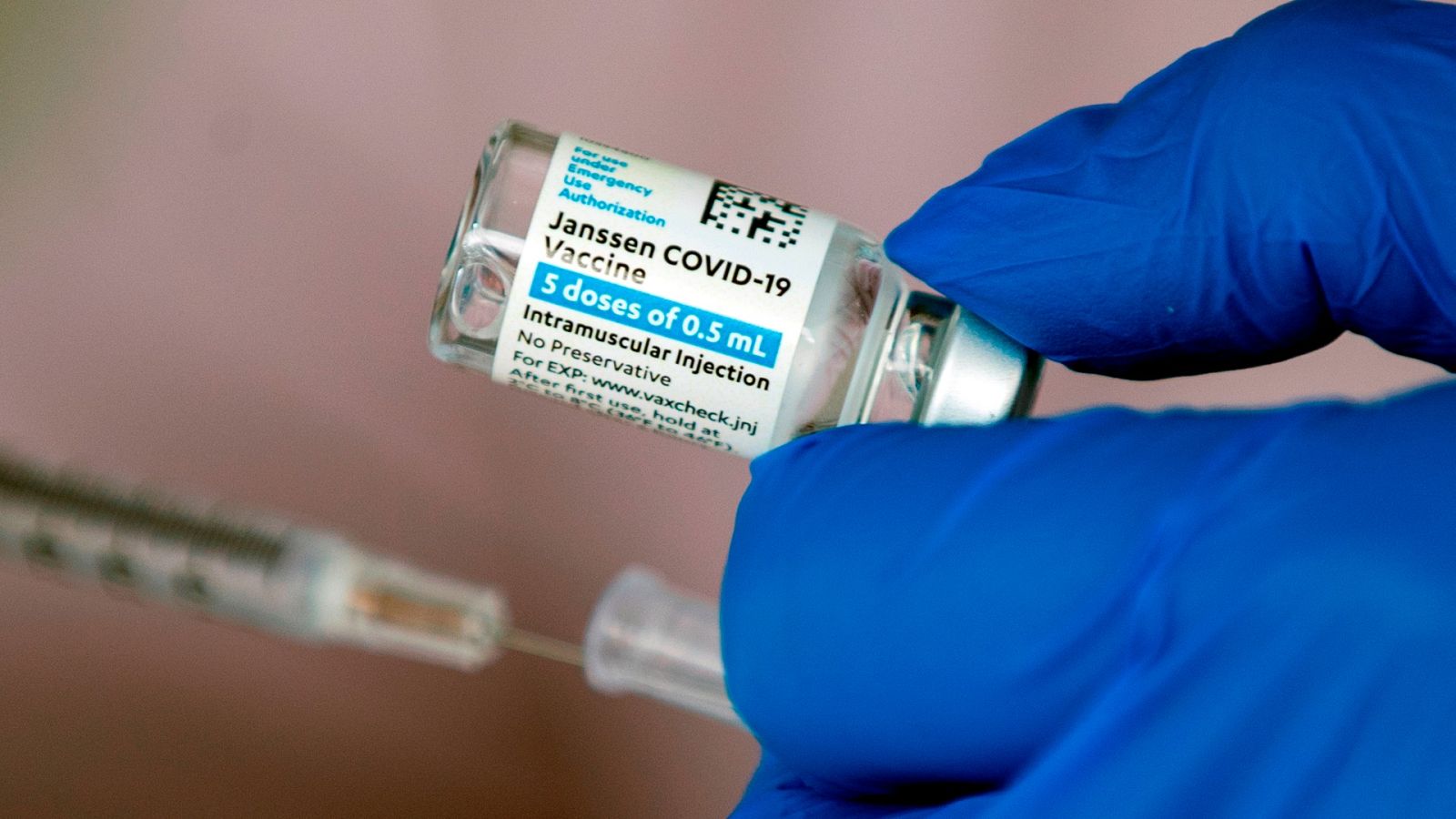
Sanidad esperará a la valoración de la EMA para administrar las vacunas de Janssen: "Vamos a ser prudentes"
España esperará a que la Agencia Europea del Medicamento (EMA) emita su informe sobre la seguridad de la vacuna de Janssen contra el coronavirus para comenzar a distribuirlas y administrarlas, después de que algunos casos de trombos paralizaran la campaña en Estados Unidos. "Vamos a ser prudentes", ha confirmado la ministra de Sanidad, Carolina Darias, tras la reunión del Consejo Interterritorial del Sistema de Salud con las comunidades autónomas.
Las primeras 146.000 dosis de la vacuna monodosis producida por la filial de Johnson&Johnson ya han llegado a nuestro país, aunque con un día de retraso, porque la compañía suspendió los envíos a Europa al conocer el aviso de las autoridades sanitarias estadounidenses.
El Gobierno mantiene sus objetivos para verano
No obstante, Darias ha enfatizado su optimismo respecto a la marcha de la campaña de vacunación y ha asegurado que el Gobierno mantiene su objetivo de inmunizar al 70 % de la población para finales de agosto. Si bien, se contaba con hasta 300.000 vacunas de Jassen solo para este abril, este miércoles la Comisión Europea ha anunciado la compra de 50 millones de dosis de Pfizer más. Por población, a España le corresponderían en torno a 5 millones del preparado que se basa en la técnica ARNm.
En pausa en Europa sin siquiera haber arrancado, la vacuna de Janssen usa un adenovirus como vector viral como AstraZeneca, y Sanidad adoptó la decisión de destinarla a inmunizar a personas de 79 a 70 años. Sobre el riesgo de retrasar la protección de este grupo de edad, vulnerable a la COVID-19, la ministra ha recordado que también se les está administrando las dosis de Pfizer y Moderna, ambas ARNm. "Si la EMA da el visto bueno a la vacuna de Janssen, iríamos vacunando de 80 hacia abajo y con la de AstraZeneca de 60 hacia arriba", ha explicado.
Las autoridades sanitarias estadounidenses emitieron este martes una declaración en la que recomendaron "una pausa en el uso de esta vacuna por precaución" mientras analizan si algunos casos de coágulos sanguíneos muy inusuales, pero "graves", están relacionados con el fármaco de Janssen. "En este momento, estos eventos adversos parecen ser extremadamente raros", aseguraron desde la FDA.
Al mismo tiempo, la EMA también ha estado investigando estos efectos desde que recibió una "señal de seguridad" a raíz de cuatro casos graves de coagulación sanguínea con plaquetas bajas en sangre tras la vacunación con este preparado, como ocurrió con AstraZeneca. El organismo regulador de la Unión Europea ha indicado este miércoles que espera poder tener su dictamen "la próxima semana", al tiempo que ha insistido en su "opinión" de que los beneficios superan a los riesgos.
Con la vacuna de AstraZeneca, hace unas semanas, la EMA acabó confirmando un "posible vínculo" con los casos inusuales de coagulación sanguínea con bajas plaquetas detectados en personas que recibieron la vacuna. El comité de seguridad (PRAC) reconoció que "debían incluirse como efectos secundarios muy raros" de la vacuna de desarrollada por la Universidad de Oxford, aunque, de nuevo, recalcó que los beneficios son muy superiores a los riesgos de efectos secundarios.
Tras este dictamen de los técnicos europeos, el Gobierno y las comunidades autónomas acordaron que las dosis de AstraZeneca se destinarían a personas a mayores de 60 años, donde los trombos son aún menos frecuentes.
"Las vacunas van a cambiar nuestras vidas. Es nuestra mejor herramienta de política sanitaria, pero especialmente nuestra herramienta más potente de recuperación económica", ha zanjado Carolina Darias, que ha señalado se han administrado 11,4 millones de dosis de la vacuna contra la COVID-19, con más de 8,2 millones de personas con una dosis y 3,1 millones de personas con dos dosis.