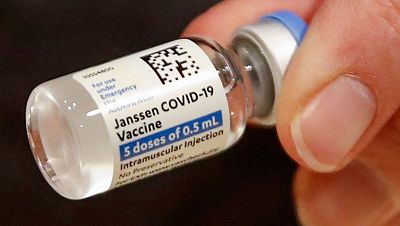
Luz verde en Estados Unidos a la reanudación del uso de la vacuna de Janssen
- EE.UU. recomendó el 13 de abril suspender el uso del suero de J&J tras detectarse seis casos de trombosis
- Coronavirus: última hora en directo | Mapa de España | Hospitales y UCI
- Vacunas en España | Guía de restricciones | Mapa mundial | Especial: La gran vacunación


Estados Unidos ha autorizado este viernes la reanudación "de inmediato" del uso de la vacuna, filial belga de Johnson&Johnson (J&J), después de que su administración quedase prácticamente suspendida hace diez días por varios casos de trombosis en mujeres.
La decisión la ha tomado la Administración de Medicamentos y Alimentos de Estados Unidos (FDA, en inglés), el organismo regulador, poco después de que un comité asesor de los Centros para la Prevención y Control de Enfermedades (CDC, en inglés) lo aconsejase este mismo viernes.
"Hemos concluido que los beneficios conocidos y potenciales de la vacuna (de Johnson&Johnson) contra la COVID-19 superan sus riesgos conocidos y potenciales en personas de 18 años o mayores", ha afirmado en una rueda de prensa la directora en funciones de la FDA, Janet Woodcock.
"Estamos seguros -ha añadido- de que esta vacuna sigue cumpliendo con nuestros estándares de seguridad, eficacia y calidad".
En esa misma rueda de prensa, el doctor Peter Marks, un alto funcionario de la FDA, ha explicado que la reanudación tiene efecto "inmediato", aunque a la práctica será efectiva este sábado por la mañana.
También ha explicado que a las personas que opten por la vacuna de J&J se les proporcionará una advertencia en papel sobre sus posibles riesgos.
Advertencia para mujeres de menos de 50 años
Los científicos del Comité Asesor sobre Prácticas de Inmunización (ACIP, en inglés) de los CDC sugirieron que ese aviso diga que las mujeres con menos de 50 años deberían estar al tanto de posibles trombos por la vacuna.
Estados Unidos recomendó el pasado 13 de abril suspender la administración del suero de J&J, después de que se detectaran seis casos de trombosis cerebral en mujeres menores de 48 años, de las que una falleció.
Hasta este viernes los CDC habían documentado quince casos confirmados en vacunadas con J&J en un abanico más amplio de edades y con un total de tres muertas.
Durante la sesión de ACIP, que duró seis horas, los científicos barajaron cuatro opciones a la hora de actualizar la recomendación.
Las alternativas iban desde desaconsejar completamente su uso a recomendarlo para todas las edades y sexos, pasando por advertir a las mujeres menores de 50 años de posibles riesgos de trombosis cerebral o sugerir su administración solo a adultos mayores de esa edad.

Sede de los CDC en Atlanta (Estados Unidos).
La mayor parte de las pacientes que presentaron trombos tras ser inmunizadas están en la treintena, aunque ha habido casos en mujeres de entre 18 y 59 años. Todas las afectadas, menos dos, tenían menos de 50 años.
15 casos de trombos y tres muertas en EE.UU.
Durante la sesión de ACIP, el médico Tom Shimabukuro, responsable de seguridad de vacunas de los CDC, explicó que entre esas quince pacientes todavía siete están hospitalizadas, de las que cuatro se encuentran en unidades de cuidados intensivos.
Precisó que trece tenían entre 18 y 49 años, y doce de ellas desarrollaron trombosis cerebrales, aunque muchas presentaron coágulos en otras partes del cuerpo.
El síntoma inicial fue dolor de cabeza, que normalmente comenzó a los seis días de haber sido vacunadas, aunque, conforme pasó el tiempo, las pacientes presentaron náuseas, vómitos, dolor abdominal, debilidad en un lado del cuerpo, dificultades para hablar, pérdida de la consciencia y espasmos, detalló el médico.
Shimabukuro destacó que siete de las mujeres eran obesas, dos tenían hipotiroidismo, dos presentaban tensión alta y otras dos estaban tomando anticonceptivos.
No está claro por el momento si alguno de esos factores podría contribuir a aumentar el riesgo de desarrollar trombos.
Por ahora se han inyectado más de 8 millones de dosis de J&J en EE.UU. , cuya administración prácticamente se ha pausado en el país tras la recomendación del pasado día 13.
Shimabukuro dijo que podría haber casos potenciales en hombres, que actualmente se están estudiando.
En concreto, el científico mencionó a un paciente de 25 años que desarrolló un coágulo cuando participó en los ensayos clínicos de la vacuna.
En la reunión participaron, además, representantes de J&J que aseguraron que se están tomando esos casos "muy seriamente".
Asimismo, revelaron antes de la votación de ACIP, que habían acordado con la FDA añadir al etiquetado un aviso de que se puede sufrir el riesgo de coágulos de sangre.
Los riesgos de J&J y AstraZeneca
En el encuentro virtual, el médico Michael Streiff, experto en trombos de la Escuela de Medicina de la Universidad Johns Hopkins, señaló que, de acuerdo a los datos que maneja, los sueros de J&J y de AstraZeneca provocan coágulos en algunas personas.
"Hasta ahora parece que hay una respuesta con trombos cuando se recibe una vacuna con vector adenoviral contra el SARS-Cov-2", detalló Streiff, quien subrayó que por el momento no está claro el motivo de esa reacción.
Tanto la vacuna de J&J como la de AstraZeneca, que aparentemente ha causado también casos de trombos en Europa, han sido desarrolladas a través de la modificación de un adenovirus, a diferencia de otras como las de Pfizer y Moderna, que han empleado una tecnología basada en ARN mensajero.
EE.UU. ha concedido autorización para uso de emergencia a los sueros de Pfizer, Moderna y J&J, mientras que AstraZeneca no ha solicitado aún ese permiso.
Hace tres días, la Agencia Europea del Medicamento (EMA) encontró un "posible vínculo" entre el desarrollo de coágulos sanguíneos muy raros y la vacuna de J&J, pero confirmó que el balance entre beneficio y riesgo de este preparado sigue siendo "positivo".
Tras dos semanas de investigaciones sobre los casos detectados en EE.UU., la EMA decidió añadir al prospecto de la vacuna una advertencia del posible riesgo, muy pequeño, de desarrollar coagulación sanguínea, pero sigue recomendando su uso en la Unión Europea (UE).