La EMA comienza a estudiar los datos sobre la dosis de refuerzo de la vacuna de Pfizer
- Moderna también ha enviado al regulador europeo la documentación necesaria para que evalúe una tercera dosis
- Coronavirus: última hora | Curva por comunidades | Hospitales y UCI | Mapa mundial
- Guía de restricciones | Vacunas en España | Vacunas en el mundo | Especial: La gran vacunación
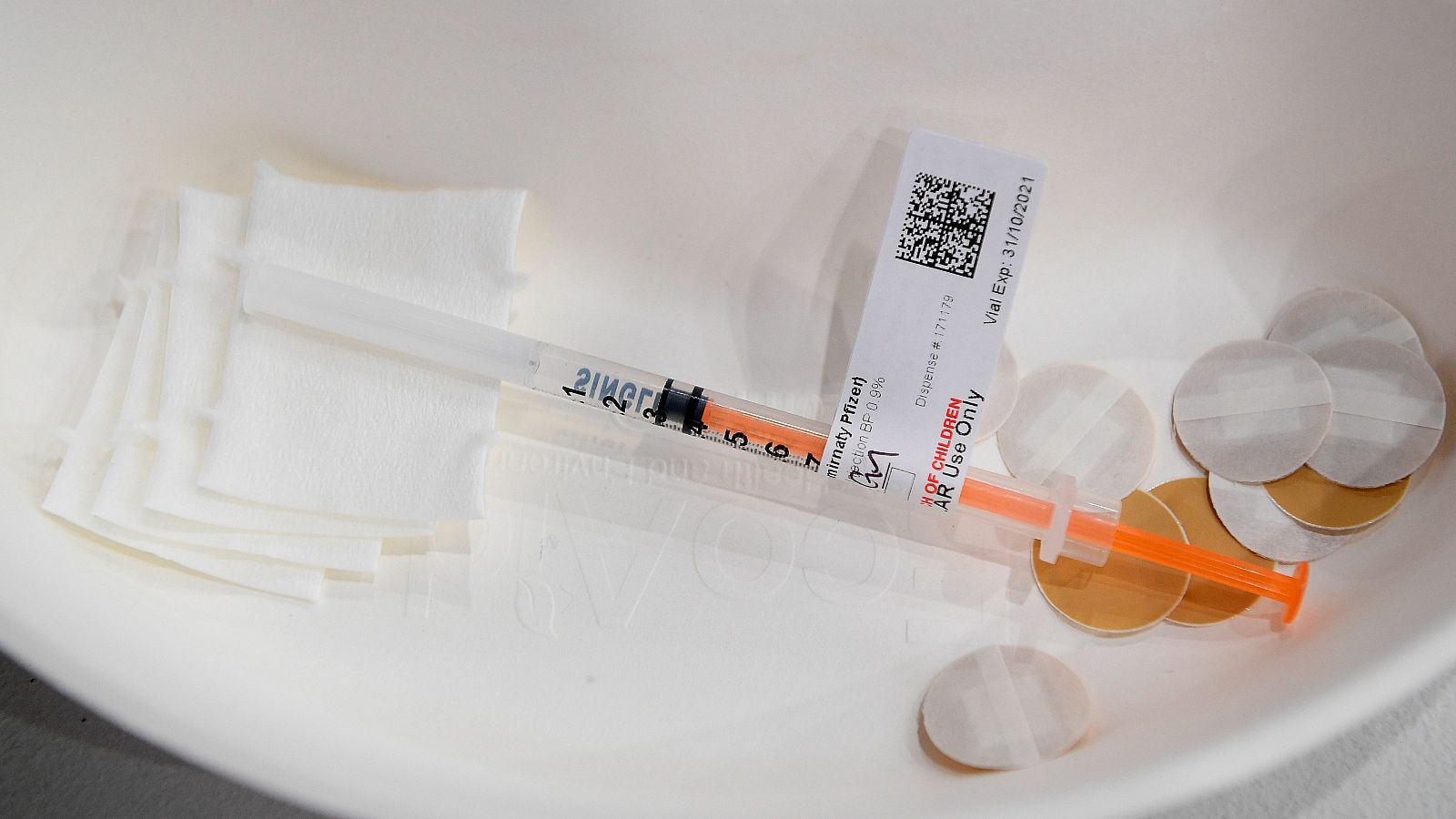

La Agencia Europea de Medicamentos (EMA) ha comenzado este lunes a evaluar la solicitud presentada por las farmacéuticas Pfizer y BioNtech para la administración un pinchazo de refuerzo seis meses después de la segunda dosis en los mayores de 16 años, y espera anunciar sus conclusiones “en las próximas semanas, a menos que se necesite información adicional” sobre la urgencia y conveniencia de la tercera dosis, y en caso positivo, se actualizará la información del producto.
El comité de medicamentos humanos (CHMP) analizará, en una evaluación acelerada, los datos presentados por estas empresas, incluidos los resultados de un ensayo clínico en marcha en el que alrededor de 300 adultos con sistemas inmunitarios sanos recibieron una tercera dosis aproximadamente seis meses después de la pauta actual recomendada.
La dosis de refuerzo de Comirnaty (nombre comercial de la vacuna de Pfizer) estaría destinada a personas que han recibido ya las dos inyecciones, es decir, que han “completado su vacunación primaria”, y tendría el objetivo de “restaurar la protección después de que haya disminuido” por el paso del tiempo.
Por otro lado, la EMA también está revisando datos sobre el uso de una dosis adicional de una vacuna de ARNm -Pfizer y Moderna- en personas severamente inmunodeprimidas, es decir, individuos con sistemas inmunológicos debilitados que no alcanzaron un nivel de protección adecuado con la pauta completa recomendada.
La agencia no ha fijado una fecha para concluir esta evaluación, que podría terminar en la recomendación de una “dosis adicional” como parte de la vacunación primaria de las personas inmunodeprimidas, en un intento de que desarrollen la protección necesaria contra la COVID-19.
El regulador europeo todavía no ha emitido una recomendación oficial sobre la tercera dosis, aunque su posición actual es la misma que la del Centro Europeo para la Prevención y Control de Enfermedades (ECDC), que comunicó la semana pasada que se debería inyectar una “dosis adicional” a las personas inmunodeprimidas, pero “no consideró urgente la necesidad de una dosis de refuerzo” en la población general.
Moderna envía los datos a la EMA
Este lunes, Moderna también ha enviado al regulador europeo la documentación necesaria para que evalúe la aprobación de comercialización condicional de una dosis de refuerzo de su vacuna mRNA-1273.
"El estudio de Fase 2 enmendado y los análisis adicionales muestran que una dosis de refuerzo de 50 ug de nuestra vacuna COVID-19 induce fuertes respuestas de anticuerpos contra la variante Delta", ha señalado Stéphane Bancel, director ejecutivo de Moderna.
El estudio de fase 2 de mRNA-1273 se modificó para ofrecer una dosis de refuerzo de mRNA-1273 al nivel de dosis de 50 ug a los participantes, seis meses después de su segunda dosis. Los títulos de anticuerpos neutralizantes habían disminuido significativamente antes del refuerzo aproximadamente a los seis meses.
Después de una tercera dosis, se logró un nivel similar de anticuerpos neutralizantes en todos los grupos de edad, especialmente en los adultos mayores (65 años o más). El perfil de seguridad después de la dosis 3 fue similar al observado previamente para la dosis 2 de ARNm-1273. Estos datos se enviarán a una publicación revisada por pares.
Un análisis adicional mostró que una dosis de refuerzo de ARNm-1273 indujo respuestas robustas para todas las variantes de interés, incluida Beta, Gamma y Delta.